
이상지질혈증은 보통 증상이 없으므로 치료가 필요한 사람을 찾아내기 위해서는 선별 검사가 필수적이다. 선별 검사를 통한 이상지질혈증 진단을 위하여 21세 이상의 모든 성인의 경우와 조기 심혈관질환과 심한 이상지질혈증의 가족력 등의 다른 위험요인이 있을 경우 더 젊은 연령에서도 적어도 매 4–6년마다 공복 후 지질 검사로, 총콜레스테롤, 중성지방, HDL 콜레스테롤, LDL 콜레스테롤(중성지방이 400 이하일 경우는 Friedewald공식으로 계산 또는 직접 측정), 그리고 non-HDL 콜레스테롤을 측정하여 이상지질혈증 평가를 시행하는 것을 권장한다.
만약 공복이 아닌 상태에서 혈청 지질 검사가 시행된 경우, 총콜레스테롤과 HDL 콜레스테롤 농도 값만 지질 상태 평가에 사용할 수 있다. 공복이 아닌 상태에서 측정한 non-HDL 콜레스테롤 농도 값이 220 mg/dL 이상인 경우 가족성 고콜레스테롤혈증일 수 있으므로 감별진단을 위한 추가 검사가 필요하다. 또한 공복이 아닌 상태에서 측정한 중성지방 농도 값이 500 mg/dL 이상인 경우 공복 후 지질 패널 검사를 권장한다. 이상지질혈증의 치료방침을 결정하기 위해서는 서로 다른 시점에 최소 2회 이상의 지질 검사가 필요하며, 만약 두 번째 지질 검사 결과와 첫 번째 검사 결과 간에 현저한 차이가 있을 경우에는 세 번째 지질 검사를 시행하여 최종 확인한 지질 검사 결과 값에 따라 치료방침을 정해야 한다.
지질 검사 항목 중에서 중성지방 값과 LDL 콜레스테롤 계산 값의 경우 혈액 채취 전 반드시 12시간 이상 금식하여야 한다. 환자가 12시간 금식이 어려운 경우 최소 9시간 이상의 금식이 필요하며, 이러한 경우 12시간 금식한 경우에 비하여 Friedewald LDL 콜레스테롤 계산 값이 약 2–4% 감소한다. 정맥 채혈 전 과도한 움직임으로 인한 혈액 농축을 피하기 위하여 최소 5분 이상 앉아 있어야 한다. 혈액 채취 용기는 혈청 검체를 검사에 사용할 경우 항응고제가 없는 튜브를 사용하고, 혈장 검체를 사용할 경우 EDTA 튜브 사용을 권장한다. 혈장 검체를 사용할 경우 혈청 검체에 비하여 약 3% 낮은 결과 값을 보인다.
이상지질혈증 진단을 위한 지질 검사 시 가능한 검사 대상자의 뇌졸중, 외부 손상, 수술, 급성감염, 체중 감소, 임신, 최근 식사의 변화 등을 피하고 최대한 안정한 상태에서 시행하는 것을 권장한다. 상기 요인들로 인하여 지질 검사 결과가 검사 대상자의 평소 지질 상태를 반영하지 못할 수 있다.
LDL 콜레스테롤 농도 값은 일반적으로 공복 후 총콜레스테롤, 중성지방, HDL 콜레스테롤 농도 값으로부터 추정할 수 있다. 즉, 검사 대상자의 중성지방 농도가 400 mg/dL 이하인 경우, 중성지방 농도 값을 5로 나누어 VLDL 콜레스테롤 농도 값을 추정할 수 있다. 총콜레스테롤은 LDL 콜레스테롤, HDL 콜레스테롤, VLDL 콜레스테롤의 총합이므로, LDL 콜레스테롤 농도 값은 다음의 Friedewald 공식으로 계산할 수 있다.

하지만 검사 대상자의 중성지방 농도 값이 400 mg/dL를 넘는 경우에는, 상기 공식에 의한 LDL 콜레스테롤 농도 값의 정확도가 떨어진다. 이러한 경우 LDL 콜레스테롤 직접 측정법(LDL cholesterol direct assay)을 권장한다. 또한 보다 정확한 LDL 콜레스테롤 농도 값 측정이 필요한 경우 미국 CDC에서 개발한 LDL 콜레스테롤 참고 검사법(LDL cholesterol beta-quantification reference measurement procedure)을 사용할 수 있다. 이와 더불어 검사 대상자의 고중성지방혈증 원인에 대한 추가 조사가 필요하다.
검사 대상자가 12시간 공복 상태가 아닌 상태에서 채혈한 경우 LDL 콜레스테롤 직접 측정법을 이용하여 지질 검사 평가를 시행할 수 있다. 하지만 최근 연구에서 Friedewald 공식을 이용하여 계산한 LDL 콜레스테롤 농도 값이 직접 측정한 값에 비하여 통계적으로 유의하게 낮음을 보고하고 있어, 이상지질혈증 진단과 치료 시 이에 대한 고려가 필요하다. 특히 동일 검사 대상자에 대한 반복 검사나 추적 관찰의 경우에는 각각의 LDL 콜레스테롤 농도 값의 산출 방식에 대한 확인이 필요하다.
최근 한국인 38,243명(중성지방 농도 400 mg/dL 이하)을 대상으로 시행한 한 연구에서 Friedewald 공식을 이용한 LDL 콜레스테롤 계산 값이 직접 측정 값에 비하여 통계적으로 유의하게 낮은 것(9.1%±6.4%)으로 보고하였다. 이러한 차이로 인하여 이상지질혈증 진단에서 Friedewald 공식을 이용한 LDL 콜레스테롤 계산 값을 사용할 경우 직접 측정법에 의한 값을 사용한 경우에 비하여 심혈관질환 발생 위험도를 상대적으로 낮게 평가할 수 있으므로 이상지질혈증 진단 및 치료 시 중성지방 농도값이 400 mg/dL 이하일 경우에도 직접측정법으로 LDL 콜레스테롤을 측정하는 것이 의미가 있겠다. 또한 최근 임상검사실에서 사용 가능한 LDL 콜레스테롤 직접 측정법의 경우 제조사별로 검사 결과 정확도에 차이가 있음이 보고되어 이상지질혈증 진단 시 이에 대한 고려가 필요하다.
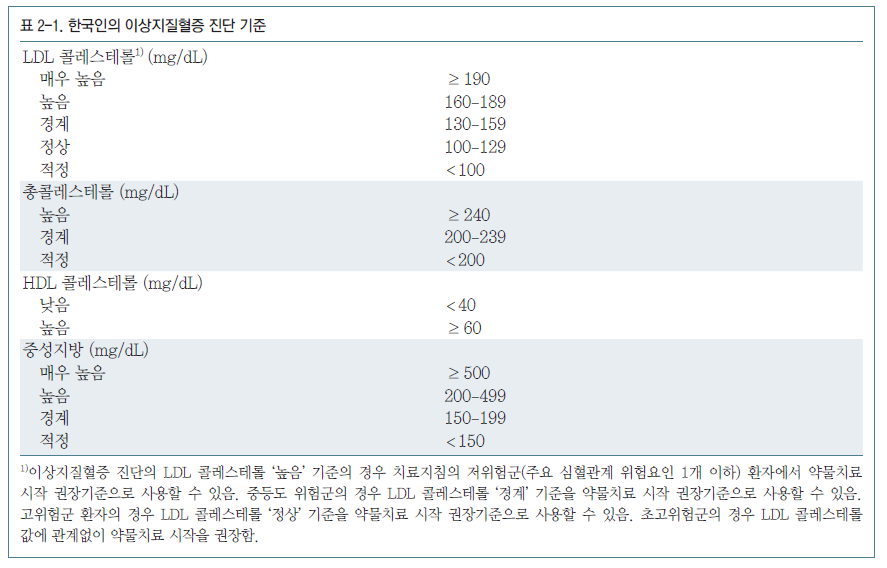
이상지질혈증 진단 기준 설정 시 근거자료로 이상지질혈증과 심혈관질환 위험도에 관한 역학연구 자료와 환자가 속한 인구집단의 지질농도 분포상에서 특정한 백분위수(percentile) 자료 등을 사용할 수 있다. 또한 이상지질혈증 치료지침에서도 이상지질혈증 농도 값 특히 LDL 콜레스테롤 농도 값을 치료방침 판단 기준에 사용하고 있어 이에 대한 고려가 필요하다. 위와 같은 사항을 고려하고, 국민건강영양조사의 결과에서 나타난 지질 농도의 분포를 감안하여 표 2-1과 같이 이상지질혈증 진단 기준을 설정하였다.

이상지질혈증 진료지침에 따른 진단 및 치료 방법 판정을 위해서는 정확하고 신뢰할 수 있는 지질 검사 결과 값의 확보가 필수적이며, 이는 각 임상검사실의 지질 검사 수행 능력에 따라 결정된다. 현재 국제적으로 이상지질혈증 진단 및 치료방침 결정을 위하여 최소한으로 요구되는 임상검사실의 지질 검사 수행 능력 평가를 위하여 미국 NCEP (National Cholesterol Education Program)에서 권장하는 지질 검사 수행능 판정 기준이 가장 널리 사용되고 있다(표 2-2). 향후 국내 임상검사실의 지질 검사 수행능 평가 연구 등을 통하여 국내 실정에 맞는 지질 검사 수행능에 대한 적절한 평가 기준의 마련이 필요할 것으로 판단된다.


1) 서론
미국에서는 2004년 Adult Treatment Panel III (ATP III) 치료지침이 개정된 후에 최근 2013년 ACC/AHA 치료지침이 새롭게 발표되었다. 새롭게 발표된 ACC/AHA 치료지침은 ‘4 statin benefit group’으로 기준을 단순화하여 스타틴 투약 여부를 쉽게 정할 수 있게 했다는 장점이 있으나 여러 가지 문제로 인하여 실질적으로 적용하는 데에는 어려움이 있을 것으로 보고된 바 있다. 한국인에게 있어서도 아래와 같은 문제들로 인하여 ACC/AHA 치료지침을 그대로 국내에 적용하는 것은 적합하지 않을 것으로 생각된다.
2013 ACC/AHA 치료지침에서는 LDL 콜레스테롤의 목표 기준을 정하지 않고 위험도에 따라 LDL 콜레스테롤 농도를 약 50% 이상 강하시킬 것으로 예상되는 고강도 스타틴 혹은 30–50%가량 강하시킬 것으로 예상되는 중간강도 스타틴을 투약할 것을 추천했으나, 이와 같은 투약 강도에 따른 지질 강하 정도는 환자에 따라 차이가 크기 때문에 기존의 치료목표를 없애고 일괄적으로 중등도 이상 용량의 스타틴을 투약하는 것은 근거가 부족할 것으로 생각된다. 또한, 치료지침이 아시아인을 대상으로 한 연구를 포함시키지 않았다는 점을 고려했을 때 우리나라를 비롯한 아시아에서 이와 같은 고강도 투약의 이점 및 부작용에 관한 연구가 필요할 것으로 생각된다.
또한 2013 ACC/AHA 치료지침에서는 기존의 심혈관질환 및 당뇨병이 없는 40세에서 75세까지의 환자에서 일차 예방을 위한 스타틴 제제의 투약을 10년 atherosclerotic cardiovascular disease (ASCVD) 위험도 7.5% 이상으로 정하였는데 실제로 이와 같은 일차 예방의 기준이 유럽이나 아시아 인구에서는 심혈관질환 위험을 과대 추정한다고 보고된 바 있다. 실제로 ACC/AHA에서는 위험도를 계산하는 데에 있어 African-American에 대한 위험도는 포함시켰지만 미국 내의 아시아인에 대한 위험도는 계산에 포함되어 있지 않기 때문에 아시아인에 적용하기 어려운 한계가 있다.
위와 같은 이유 및 최근 새롭게 발표된 연구 결과들을 고려해 국내에 맞는 치료 기준을 다시 정해야 할 필요성이 대두되었다. 치료방침을 정하는 데 있어서 현재까지는 한국인의 대규모 코호트를 통한 심혈관계 위험도 평가와 같은 자료가 부족하기 때문에 기존의 국내 및 외국 지침들을 참고하여 기준을 설정하는 것이 필요할 것으로 생각된다.
2) 새로운 한국인에서의 치료 기준
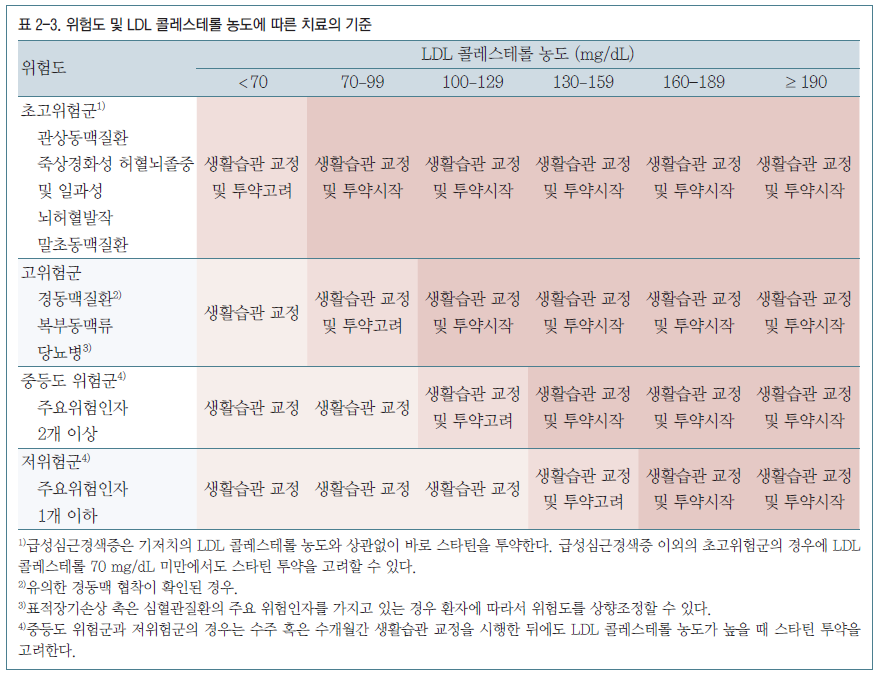
새로운 국내 치료지침에서는 기존에 국내의 치료지침에서 제시했던 대로 심혈관계 위험요인들의 유무를 판단하여 위험 수준에 따라 목표 LDL 콜레스테롤 농도를 차등 설정하는 틀을 유지하되, 구체적인 위험요인들이나 치료 기준에 관해서는 국내 및 국외의 연구 결과와 2013년 ACC/AHA, 2016년 European Society of Cardiology (ESC)/European Atherosclerosis Society (EAS) 및 각국의 치료지침을 참고하여 수정 및 보완하는 것으로 정하였다(표 2-3, 2-4).
텍스트 추가
대표사진 삭제
사진 설명을 입력하세요.
텍스트 추가
(1) 초고위험군
기존에 심혈관질환이 있는 환자(관상동맥질환, 말초동맥질환, 죽상경화성 허혈뇌졸중 및 일과성 뇌허혈발작)를 초고위험군 환자로 따로 분류하여, 이 경우 이차 예방을 위해 LDL 콜레스테롤 70 mg/dL 미만 혹은 기저치보다 50% 이상 감소를 목표로 하는 것을 권고한다(I, A).
이전 국외의 연구에서 LDL 콜레스테롤 농도가 130 mg/dL 미만인 안정성 협심증 환자 만 여 명을 대상으로 저용량 혹은 고용량 스타틴을 투약한 무작위 배정연구에서 고용량 투약 뒤 LDL 콜레스테롤을 70 mg/dL에 가깝게 낮춘 경우 심혈관질환 위험도를 약 22% 가량 낮춘다고 보고한 바 있으며 스타틴을 투여한 환자를 메타 분석한 결과에서도 LDL 콜레스테롤을 70 mg/dL 미만 혹은 기저치에 비해 50% 이상 감소시켰을 때 가장 심혈관질환의 예방효과가 큰 것으로 확인된 바 있다. 하지만, 최근 10일이내 급성관동맥증후군이 발생했던 17,706명 환자를 대상으로 진행되었던 Improved Reduction of Outcomes: Vytorin Efficacy International Trial (IMPROVE- IT)에서는 중등강도 스타틴과 에제티미브 병용요법이 중등강도 스타틴 단독요법에 비해 주요 심혈관 사건의 상대위험도를 6.4%가량 낮추었다. 연구기간 동안 LDL 콜레스테롤 수치는 스타틴 단독요법군이 69.9 mg/dL, 병용요법군이 53.2 mg/dL로, LDL 콜레스테롤을 70 mg/dL 미만으로 낮추었다 할지라도 추가적인 LDL 콜레스테롤의 감소가 주요 심혈관 사건의 위험도를 낮춘다는 것을 보고하였다. 이 연구 결과를 토대로 최근 2018 AACE/ACE에서는 죽상동맥경화성 심혈관질환을 가지는 환자로서, 1) LDL 콜레스테롤이 70 mg/dL 미만으로 도달하였다 하더라도 죽상동맥경화성 심혈관질환이 진행하는 경우, 2) 당뇨병 환자, 3) 만성콩팥병 3기와 4기 환자, 4) 이형접합 가족성 고콜레스테롤혈증 환자, 5)조기 죽상동맥경화성 심혈관질환의 병력(남자 55세 미만, 여자 65세 미만)이 있는 환자들을 극초고위험군(extreme risk)으로 분류하여 LDL 콜레스테롤의 목표수치를 55 mg/dL미만으로 낮출 것을 권고하고 있다.
또한, 스타틴을 투여 중 LDL 콜레스테롤이 70 mg/dL이상인 죽상동맥경화성 심혈관질환이 있는 27,564명의 환자를 대상으로 진행한 Further Cardiovascular Outcomes Research with PCSK9 Inhibition in Subjects with Elevated Risk (FOURIER)연구에서는 대상자의 80% 이상이 과거 심근경색증의 기왕력이 있었던 환자들이었고, proprotein convertase subtilisin-kexin type 9 (PCSK 9)억제제인 evolocumab의 효과를 평가하였다. evolocumab 투여군의 LDL 콜레스테롤의 중앙값은 30 mg/dL이었고, evolocumab 투여군이 위
텍스트 추가

대표사진 삭제
사진 설명을 입력하세요.
텍스트 추가
약대조군에 비해 주요 심혈관 사건의 위험도를 15% 의미 있게 감소시켜주었다. 최근 또 다른 PCSK9 억제제인 Alirocumab에 대한 연구인 ODYSSEY OUTCOMES 연구에서도 급성관동맥증후군이 발생한지 1개월에서 12개월 사이 고강도 스타틴 치료를 받는 18,900여 명 환자들에서 alirocumab투여군은 위약대조군에 비해 주요 심혈관 사건의 위험도를 15%가량 감소시켰고, alirocumab군에서의 LDL 콜레스테롤수치는 연구시작 4개월째 37.6 mg/dL, 48개월째 53.3 mg/dL로 측정되었다. 위의 세 가지 연구는, 특히 초고위험군에서 LDL 콜레스테롤의 목표 수치를 기존의 수치보다 낮추는 것이 부가적으로 주요 심혈관 사건의 개선에 도움이 된다는 것을 입증한 바, 임상적으로 명백한 죽상동맥경화성 심혈관질환(특히 급성관동맥증후군)이 있는 환자에서 LDL 콜레스테롤의 목표 수치를 현재의 지침보다 하향 조정하는 것이 필요할 수 있음을 시사한다. 하지만 비용효과관련 연구와 향후 국내 연구가 필요할 것으로 생각된다.
또한 6개월 내에 허혈성 뇌졸중 및 일과성 뇌허혈발작이 발생했던 4,700여 명의 환자를 대상으로 진행된 국외의 무작위 배정 연구에서 스타틴 투여 군에서의 LDL 콜레스테롤 농도가 73 mg/dL, 위약군에서는 129 mg/dL로 확인되었으며 스타틴을 투여한 경우 위약에 비해 뇌졸중의 위험 및 심혈관질환의 위험도가 각각 16%, 20%로 유의하게 감소됨을 보고한 바 있어 허혈성 뇌졸중 환자에서도 스타틴의 투약을 통해 LDL 콜레스테롤을 70 mg/dL에 가깝게 낮추는 것이 도움이 될 것으로 생각되었다. 그러나 국내의 Korea Medical Insurance Corporation (KMIC) 연구 및 일본의 NIPPON DATA80 코호트에서 고콜레스테롤혈증보다 고혈압이 뇌혈관질환과의 관련성이 컸던 점 및 고용량 스타틴 투약 뒤 허혈성 뇌졸중은 감소하나 출혈성 뇌졸중은 증가했던 이전 보고를 고려했을 때 허혈성 뇌졸중을 예방하기 위한 스타틴 용량 및 LDL 콜레스테롤 목표에 대해서는 향후 국내 연구가 필요할 것으로 생각된다.
이전 지침에서는 경동맥질환에 의한 일과성 뇌허혈발작이 경동맥 협착과 같이 고위험군 범주에 포함되어 있었으나 이후 발표된 연구들에서 일과성 뇌허혈발작 환자의 상당수에서 향후 뇌졸중 및 심혈관질환 발생이 증가하기에 일과성 뇌허혈발작 환자를 뇌졸중 환자와 같은 위험도를 가진 것으로 평가해야 한다고 보고된 바 있었다. 이전 일과성 뇌허혈발작 및 뇌졸중 환자를 대상으로 퇴원 후 6개월 뒤 뇌졸중의 재발 여부를 확인한 연구에서 일과성 뇌허혈발작 환자에서의 뇌졸중 발생률은 5%, 뇌졸중 환자에서의 재발률은 6%로 두 군 간에 차이가 없음이 보고된 바 있었다. 또한 일과성 뇌허혈발작이 발생했던 약 2,400여 명의 환자를 대상으로 코호트 연구를 했던 Dutch TIA Trial에서 10년간 환자들을 추적 관찰한 결과 약 54%의 환자가 적어도 1개 이상의 심혈관질환(뇌졸중, 심근경색 및 심혈관질환으로 인한 사망)이 발생했다고 보고된 바 있었다. 따라서 현재까지 일과성 뇌허혈발작 환자에서 LDL 콜레스테롤의 목표를 어떻게 정하고 스타틴을 투약할지에 대해서는 정해진 바가 없으나 이전 뇌졸중과 일과성 뇌허혈발작이 발생한 환자를 대상으로 했던 연구들에서 고용량 스타틴 투약이 심혈관질환 위험도를 낮추었던 점 및 이와 같은 환자군에서 향후 심혈관질환 발생위험이 높음을 고려하여 이번 지침에서는 일과성 뇌허혈발작을 뇌졸중과 같은 초고위험군으로 분류하였다.
또한 이전 말초동맥질환 및 관상동맥질환, 당뇨병이 있는 2만 명의 환자를 대상으로 한 무작위 배정 연구에서(Heart Protection Study) 스타틴을 투여하는 경우 위약군에 비해 심혈관질환이 유의하게 감소하는 것이 확인되었으며 추가분석에서 기저 LDL 콜레스테롤 농도가 116 mg/dL 미만이며 스타틴 투약 뒤 LDL 콜레스테롤 농도가 70 mg/dL로 감소했던 군에서도 스타틴 투여 뒤 심혈관질환의 위험이 유의하게 감소하는 것이 확인되었기에 말초동맥질환 군 또한 초고위험군으로 분류하였다.
급성심근경색증이 발생한 경우에는 기저치의 LDL 콜레스테롤 농도와 상관없이 바로 스타틴을 투여하는 것을 권고하는데(I, A), 이전 국외에서 진행된 약 4,500여 명의 급성심근경색증 환자를 대상으로 한 무작위 배정 연구에서 심근경색증이 발생한 후 바로 스타틴을 투여한 군에서 그렇지 않은 군에 비해 심혈관질환이 적게 발생하는 것으로 보고된 바 있으며, 국내에서도 등록 환자를 후향적으로 분석한 연구였으나 급성심근경색증 발생 시 LDL 콜레스테롤 농도가 70 mg/dL 미만이었던 환자 약 천여 명을 대상으로 바로 스타틴을 투여한 군과 그렇지 않은 군을 추적 관찰한 결과, 스타틴을 바로 투여한 군에서 1년 뒤 심혈관질환이 적게 발생하는 것으로 보고된 바가 있다. 따라서 국내 및 국외의 연구 결과를 고려했을 때, 급성심근경색증이 발생한 경우에는 기저 LDL 콜레스테롤 농도와 관계없이 즉각적으로 스타틴을 투여하는 것을 추천한다(I, A).
따라서 기존의 연구 결과를 종합했을 때, 기존에 심혈관질환(관상동맥질환, 말초동맥질환, 죽상경화성 허혈뇌졸중)이 있는 초고위험군 환자의 경우 이차 예방을 위해 일차적으로 스타틴을 투여하는 것을 권고하며(I, A), LDL 콜레스테롤의 목표에 도달되지 않을 경우 에제티미브나 PCSK 9억제제의 병용요법을 권고한다(IIa, B). LDL 콜레스테롤의 목표 수치는 70 mg/dL 미만, 혹은 기저치에 비해 50% 이상 감소로 정하는 것을 권고한다(I, B).
(2) 고위험군
이전 지침에서 고위험군으로 분류되었던 심혈관질환 과거력이 있는 환자군이 개정판에서 초고위험군으로 따로 분류되며, 이전 치료지침에서 고위험군에 해당되었던 관상동맥질환에 상당하는 위험인자인 경동맥질환이나 복부동맥류, 당뇨병이 있는 환자는 고위험군에 남아, 일차 예방을 위해 LDL 콜레스테롤 농도가 100 mg/dL 이상인 경우 치료가 권장된다(I, A).
경동맥질환이 있는 경우 심혈관계 위험이 증가하는지에 대해 이전 North American Symptomatic Carotid Endarterectomy Trial (NASCET)에서 경동맥 협착 증세로 인해 경동맥 내막절제술(carotid endarterectomy)을 받았던 1,415명의 환자를 추적 관찰한 결과 8년간 동측의 뇌졸중이 발생 위험이 17.1%가량으로 높게 확인된 바 있으며 이와 비슷하게 ECST 연구에서도 증상이 있는 경동맥 협착 환자는 경동맥 협착 정도와 상관없이 심혈관질환으로 인한 사망률이 높아 6년 사망률이 27%로 확인되었고 이를 토대로 계산된 10년간 심혈관계 사망률이 30%로 추정된 바 있다. 또한 경동맥 잡음(carotid bruit)이 청진되는 환자를 추적 관찰한 연구에서 경동맥 협착 정도에 따른 심혈관질환 발생률을 알아본 결과, 협착이 50% 미만인 군, 50–75% 사이인 군, 75% 이상인 군에서 각각 2.7%/yr, 6.6%/yr, 8.3%/yr로 확인되어 50% 이상 협착이 있는 군에서 심혈관질환의 위험도가 크게 증가함을 확인할 수 있었다. 이 외에도 증세가 없는 경동맥 협착 환자를 대상으로 한 연구들에서도 50% 이상 협착이 진행된 경우 심혈관질환이 증가하는 것으로 보고되어 ATP III 치료지침에서는 증세가 없더라도 50% 이상 협착이 진행된 경우 심혈관계 고위험군으로 분류하였다. 또한 심혈관질환이 없으면서 경동맥 협착이 있는 환자에서 lovastatin과 placebo를 투약했던 이전 연구에서 스타틴 투약군에서 LDL 콜레스테롤 농도가 156.6 mg/dL에서 113.1 mg/dL로 감소했으며 주요 심혈관계 사건 및 사망률이 감소되었던 연구 결과를 고려하여 개정된 국내 치료지침에서도 이전 방침과 같이 경동맥 협착이 있는 환자는 고위험군으로 분류하는 기준을 유지하기로 하였으나, 50%이상이라는 구체적인 협착 정도는 제외하였다.
복부대동맥류가 있는 환자가 심혈관계 위험이 증가하는지에 대한 이전 결과를 보면, 복부대동맥류 수술을 받았던 343명의 환자를 약 11년간 추적 관찰한 연구에서 수술 전 심혈관질환이 없던 환자에서도 매년 약 1.9%가량의 높은 심혈관계 사망률이 확인된 바 있다. 이에 따라 ATP III 치료지침에서는 복부대동맥류 환자를 고위험군으로 분류하였고 국내 치료지침도 이에 맞추어 복부대동맥류가 있는 군은 심혈관계 고위험군으로 분류되어 있었다. 이후에 진행된 연구들에서도 스타틴의 투약이 복부대동맥류 환자에서 대동맥류의 크기와 수술 후 단기 및 장기 사망률을 개선시키는 데에 유의한 효과가 있음이 알려진 바 있기에 이번 개정된 지침에서도 이전과 같이 복부대동맥류가 있는 경우 심혈관계 위험도의 고위험군으로 분류하고 이에 맞게 스타틴 치료를 하는 것을 유지하기로 하였다.
제1형 및 2형 당뇨병이 있는 환자에서 심혈관질환의 위험이 증가하는 것은 이전 연구들에서 이미 잘 알려진 바 있다. 제2형 당뇨병 환자 2,500여 명을 7년간 추적 관찰한 핀란드의 코호트 연구에서 당뇨병이 있으며 기존에 심혈관질환이 없던 환자의 심근경색 발생률은 20.2%로 당뇨병이 없으며 심혈관질환이 있는 환자의 18.8%와 유사하게 확인되었으며, 이후에 진행된 Organization to Assess Strategies for Ischemic Syndromes (OASIS) 연구에서도33 제2형 당뇨병이 있으면 심혈관질환의 과거력이 없더라도 심혈관질환의 과거력이 있던 환자와 비슷한 심혈관질환이 발생하는 것으로 확인되어 고위험군으로 분류되었다. 또한 제2형 당뇨병 환자에서는 심근
텍스트 추가
대표사진 삭제
사진 설명을 입력하세요.
텍스트 추가
경색 발생 시 당뇨병이 없는 환자군에 비해 사망률이 높은 것으로 알려져 있으며, 심혈관질환에 따른 예후가 나쁜 것으로 알려져 있어 심혈관질환이 발생하기 전에 미리 예방하는 것이 중요하다고 보고된 바 있다. 당뇨병이 있는 환자에서 스타틴 투약에 따른 효과에 대해 이전의 14개의 무작위 배정 연구들을 메타분석한 결과 당뇨병이 있는 환자에서 스타틴 투약 후 LDL 콜레스테롤 농도가 40 mg/dL 감소할 때마다 모든 원인에 의한 사망률이 9% 감소했으며 주요 심혈관계 위험이 21% 감소했고 이와 같은 효과는 동반된 심혈관질환의 유무와 상관없이 효과적임이 보고된 바 있었다. 또한 투약 전 LDL 콜레스테롤 농도가 100 mg/dL 미만이었으며 투약 후 80 mg/dL 미만으로 감소한 군에서도 이와 같은 효과가 유지됨이 확인되어 당뇨병이 있는 환자에서 적극적으로 스타틴을 투약하는 것이 필요함을 보여주었다.
또한 Collaborative Atorvastatin Diabetes Study (CARDS)에서 이전에 심혈관질환의 과거력이 없으면서 1가지 이상의 위험인자(당뇨병성 망막병증, 알부민뇨, 흡연, 고혈압)가 동반된 2,800여 명의 환자에게 스타틴 투약에 관한 무작위 배정연구를 진행한 결과에서 스타틴 투약군에서 위약군에 비해 심혈관질환의 위험도가 37% 감소하는 것이 확인되었으며, 투약군에서의 평균 LDL 콜레스테롤 농도가 약 80 mg/dL, 위약군에서의 평균 농도는 120 mg/dL였던 점을 고려했을 때 당뇨병이 있으면서 다른 위험인자가 동반된 경우 LDL 콜레스테롤 목표를 하향 조정하는 것이 필요할 수 있음을 시사하였다. 따라서 당뇨병 환자에서의 위험도는 표적장기손상 혹은 심혈관질환의 주요 위험인자를 가지고 있는 경우 환자에 따라 상향조정할 수 있음을 언급하였다.
이전 당뇨병 환자들을 대상으로 했던 연구들에서는 대부분 스타틴의 투약 여부 및 용량에 따른 심혈관질환의 발생을 평가했기에 이상적인 LDL 콜레스테롤 농도의 감소폭을 정확히 정하기는 어렵다. 그러나 대부분의 위약-실험군 연구들에서 스타틴 투약 뒤 LDL 콜레스테롤 농도가 30–40%가량 감소했던 것을 고려했을 때, 기저치의 LDL 콜레스테롤 농도가 매우 높아 고용량의 스타틴 투약에도 100 mg/dL 미만으로 감소되지 않는 환자의 경우라도 30–40% 이상의 감소폭을 보였다면 투약에 따른 효과가 있는 것으로 여겨진다. 제1형 당뇨병 환자에서도 심혈관질환의 위험이 증가한다는 것은 이전 연구들에서 잘 알려져 있으나 비교적 젊은 나이에 발병하는 특성이 있어 같은 나이의 당뇨병이 없는 환자에 비해 심혈관 위험도가 어떻게 다른지에 대해서는 명확하게 알려져 있지는 않다. 그러나 최근의 메타 분석에서 당뇨병의 유형과 상관없이 스타틴 투약이 심혈관계 위험을 감소시킨다는 결과가 나와 제1형 당뇨병 환자에서도 적극적인 투약이 도움이 될 수 있음을 보여주었다.
(3) 중등도 위험군
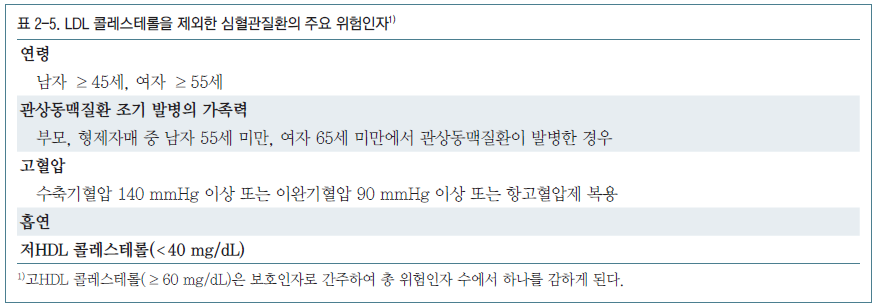
중등도 위험군의 기준은 기존의 국내 치료지침을 유지하여 LDL 콜레스테롤을 제외한 주요 위험인자(표 2-5)가 2개 이상인 경우 중등도 위험군으로 분류되며, 수주 혹은 수개월간 생활습관 교정을 시행한 후에도 LDL 콜레스테롤 농도가 130 mg/dL 이상인 경우 스타틴을 투약한다(II, B).
주요 위험인자를 구성하는 각각의 항목은 기존의 ATP III에서 정했던 위험인자 및 국내의 치료지침을 유지하였고, 이 중 흡연, 고혈압, 연령, 성별, 저HDL 콜레스테롤 등의 위험인자는 2013 ACC/AHA1 및 European Society of Cardiology and the European Atherosclerosis Society (ESC/EAS)5, Japan Atherosclerosis Society (JAS)41 등의 각국치료지침에서도 채택하고 있는 위험인자이다.
각각의 위험인자에 대해 살펴보면, 흡연은 잘 알려진 심혈관질환의 위험인자로 이전 연구들에서 흡연에 따른 심혈관질환 발생의 증가 및 금연에 따른 감소가 확인된 바 있다. 고혈압 역시 이전 여러 연구들에서 관상동맥질환 및 뇌졸중을 포함한 심혈관질환과 연관이 있음이 밝혀진 바 있다. 일본을 포함한 7개의 나라에서 혈압이 관상동맥질환으로 인한 사망률에 미치는 영향에 대해 조사한 이전 연구 결과를 보면, 인구 집단과 상관없이 고혈압이 심혈관계 사망률의 상대 위험도를 증가 시킨다고 보고되었으며, 수축기 혈압이 10 mmHg 증가할 때마다 상대위험도가 이완기 혈압이 5 mmHg 증가할 때마다 상대위험도가 1.28로 증가하는 것이 확인되었다. 또한 이전 연구에서 HDL 콜레스테롤 농도가 약 1 mg/dL가량 증가하면 심혈관질환으로 인한 사망률이 남성의 경우 3.7%, 여성의 경우 4.7% 감소하는 것으로 보고된 바 있어 연구 결과들을 바탕으로47 저HDL 콜레스테롤 농도(<40 mg/dL)가 심혈관질환의 위험 인자로 포함되었으며 고HDL 콜레스테롤(60 mg/dL)은 보호 인자로 총 위험인자 수에서 하나를 감하는 것으로 정하였다. 나이가 증가함에 따라 심혈관계 위험이 증가하는 것은 이전 연구들에 의해 잘 알려진 사실로, 여성은 남성에 비해 약 10–15년이 지난 후에 심혈관질환 위험도가 비슷해지는 것으로 알려져 있다. 이전 Framingham Heart Study에서는 이와 같은 성별에 따른 차이가 다른 위험 인자들의 차이로 전부 설명되지 않기 때문에 성별에 따라 위험 인자가 되는 나이의 기준을 다르게 하여, 남성은 45세 이상, 여성은 55세 이상인 경우 위험 인자에 해당되는 것으로 분류하였다. 또한 이전 연구들에서 심혈관질환 가족력이 있는 경우, 즉 부모, 형제자매 중 남자 55세 미만, 여자 65세 미만에서 관상동맥질환이 발병한 가족력이 있는 경우 심혈관질환이 진행될 위험이 약 2배에서 12배가량 증가한다고 보고된 바 있어 이 또한 위험인자에 포함되었다.
그러나 이와 같은 주요 위험인자들을 토대로 위험도를 평가하는 것은 실제 심혈관질환의 위험도의 약 절반 정도만 예측하는 것으로 알려져 있어23 비만, 신체활동, 식습관, 중성지방, high sensitivity C-reactive protein (hsCRP), lipoprotein (a), apolipoprotein, fibrinogen, homocysteine, apolipoprotein B, ankle-brachial blood pressure index, carotid intimal medial thickening (50% 미만의 협착이지만 임상적으로 진행 소견이 보이거나 동맥경화반이 동반된 경우), coronary calcium score 등의 다른 위험인자들을 고려하여 경우에 따라 개별화된 치료목표를 정할 수 있을 것으로 생각된다.
(4) 저위험군
LDL 콜레스테롤을 제외한 주요 위험인자(표 2-5)가 1개 이하인 경우 저위험군으로 분류되며 이전 치료지침과 같이 수주 혹은 수개월간 생활습관 개선을 시행한 뒤에도 LDL 콜레스테롤 농도 160 mg/dL 이상인 경우 스타틴을 투약한다(II, B). 개정된 지침에서는 LDL 콜레스테롤 목표를 이전 치료지침과 같이 160 mg/dL 미만으로 정했으나, 위의 중등도 위험군에서 주요 위험인자 이외에 다른 위험인자들을 고려했던 것과 같이 저위험군에서도 경우에 따라 강화된 치료목표를 정할 수 있을 것으로 생각된다(II, B). 특히 LDL 콜레스테롤 농도가 190 mg/dL 이상인 경우 고지혈증을 일으키는 다른 원인 [담도폐쇄(biliary obstruction), 신증후군(nephrotic syndrome), 갑상선기능저하증(hypothyroidism), 임신, glucocorticoid, cyclosporine 등의 투약력]이 있는지에 대해서 확인하고 교정하는 것이 필요하다.1 이차적인 원인이 없는 상태에서 LDL 콜레스테롤 농도가 190 mg/dL 이상인 경우 위험 정도와 상관없이 스타틴 투약할 것을 권고하는데 이는 2004년 개정된 ATP III50 및 2013년 ACC/AHA 치료지침1과도 일치한다(I, A).
(5) 고중성지방혈증에 대한 치료지침
혈중 중성지방 농도가 500 mg/dL 이상으로 상승되는 경우 급성췌장염의 위험이 증가한다고 알려져 있으며51 이 경우 중성지방을 증가시킬 수 있는 이차적인 원인(체중 증가, 음주, 탄수화물 섭취, 만성콩팥병, 당뇨병, 갑상선기능저하증, 임신, 에스트로겐, tamoxifen, glucocorticoid 등의 투약력) 및 지질대사의 이상을 일으킬 수 있는 유전적인 문제가 있는지 확인하는 것이 필요하다(I, A). 이차적인 원인이 없거나 교정된 뒤에도 지속적으로 500 mg/dL 이상의 중성지방 농도가 확인되는 경우 췌장염을 예방하기 위해 fibrate, nicotinic acid, omega 3 fatty acid 등의 약물치료를 시작하는 것을 권고하며(II, A) 이는 ATP III23 및 2016년 ESC/EAS5치료지침과도 일치한다.
중성지방 농도가 200–499 mg/dL이면서 LDL 콜레스테롤이 동반되어 상승되어 있는 경우에는 일차적으로 LDL 콜레스테롤 농도를 낮추기 위해 스타틴을 투약하는 것을 권고한다. 또한 이전 연구들에서 높은 중성지방 농도가 다른 위험인자와는 독립적으로 심혈관질환의 위험과 연관이 있다고 알려져 있어 중성지방 농도가 200–500 mg/dL이면서 LDL 콜레스테롤 농도가 위험군에 따른 목표치보다 낮은 경우에는 우선 생활 습관 개선을 권고하고 이후에도 고중성지방 혈증이 지속되는 경우 위험도를 고려하여 일차 약제로 스타틴을 투약할 것을 추천한다. 이 경우 치료의 목표는 이전과 같이 non-HDL 콜레스테롤 농도(=총콜레스테롤-HDL 콜레스테롤)를 계산하여 표 2-4의 기준에 따라 조정한다(II,A). 목표 non-HDL 콜레스테롤의 농도는 기존의 LDL 콜레스테롤의 목표치에 30을 더한 값이다.
고중성지방혈증 환자에서 중성지방을 낮추는 데 효과적인 fibrate 등과 같은 약제 대신 스타틴을 일차 약제로 권고하는 이유는 기존의 연구 결과들에서 스타틴 투약이 심혈관질환의 예방에 도움이 될 것으로 여러 차례 확인되었던 것을 기반으로 한다. Fibrate 투약이 심혈관질환의 예방에 도움이 되는지에 대해서는 아직 논란이 있는 상태이며 이전 무작위 배정연구들을 메타분석하여 고지혈증 치료약제의 투약이 사망률에 미치는 영향을 조사한 결과에서 스타틴은 심혈관계 사망률을 유의하게 감소시켰으나, fibrate는 위약군에 비해 사망률을 유의하게 줄이지 못했다. 한국인에서 fibrate 투약이 심혈관질환에 미치는 영향에 대해서는 추가적인 연구가 필요할 것으로 생각된다. 현재까지는 고중성지방혈증 환자에서 fibrate 투약이 statin 투약과 비교하여 심혈관계 예방 효과가 우월하다는 연구 및 보고가 없었던 점1을 고려할 때51 등을 고려할 때 고중성지방혈증으로 인한 심혈관질환의 진행을 예방하기 위해서는 스타틴이 일차 약제로 투약되는 것이 바람직 할 것으로 생각된다.
이와 같이 고중성지방혈증 환자에서 생활습관 개선 및 스타틴을 투약한 후에도 고중성지방혈증이 호전되지 않는 경우 fibrate, omega 3 fatty acid 등의 약제를 스타틴에 추가하여 투약하는 것이 심혈관질환의 위험을 낮추는지에 관해서도 아직까지 논란이 있는 상태이다. 이전 ACCORD 연구 그룹에서 기존에 스타틴을 투약하고 있는 약 5,500여 명의 제2형 당뇨병 환자를 대상으로 fenofibrate 및 위약을 추가로 투약한 뒤 4.7년간 관찰한 연구에서 추가적인 fibrate 투약이 심혈관질환 및 사망률을 줄이지 못한 것으로 보고된 바 있었으나, 이 연구에서 전체 집단의 투약 전 중성지방 농도가 162 mg/dL로 낮았으며, 연구의 추가 분석에서 중성지방 농도가 기존에 204 mg/dL 이상이며 HDL 콜레스테롤 농도가 34 mg/dL 이하로 낮았던 군에서는 심혈관질환의 발생이 투약군에서 12%, 위약군에서 17%로 차이를 보인 바 있었다. 또한 일본에서 약 18,000여 명의 고지혈증 환자를 대상으로 스타틴 혹은 스타틴과 eicosapentaenoic acid를 동시 투약 후 4.6년 후에 관상동맥질환의 발생을 알아본 JELIS 연구에서 동시 투약 군에서 위험도가 19%가량 감소하는 것이 확인되었으며, 두 군 간에 LDL 콜레스테롤 농도는 변화가 없었으나 중성지방 농도는 동시 투약 군에서 유의하게 더 감소되는 것으로 확인되어 추가 투약의 유용성을 보여준 바 있었다. 따라서 생활습관 개선 및 스타틴 투약 후에도 200 mg/dL 이상의 고중성지방혈증이 지속될 때 고위험군에 해당되는 환자의 경우 심혈관질환의 예방을 위하여 fibrate, omega 3 fatty acid 등의 중성지방 농도를 낮추는 약을 스타틴에 추가로 투약하는 것을 권고한다(II, B).
3) 결론
2013년 ACC/AHA 치료지침은 LDL 콜레스테롤 농도의 목표를 정하지 않고 일괄적으로 중등도 이상의 용량의 스타틴 투약을 추천하여 약물 반응의 개인별 차이를 반영하지 않은 점, 고용량 스타틴 투약에 따른 이점 및 부작용이 불확실한 점, 국내의 심혈관질환 위험을 과대 추정할 수 있는 점 등을 고려했을 때 국내에 적용하는 데에 문제가 있을 것으로 생각된다. 그러나 2013년 ACC/AHA 치료지침 및 최근 연구 결과를 고려했을 때 스타틴 투약의 유용성이 증명된 기저에 심혈관질환이 있거나 이에 상응하는 위험인자가 있는 환자에서는 적극적으로 스타틴 투약을 시작하는 것이 바람직하겠다. 개정된 치료지침에서는 이와 같은 요구를 반영하여 초고위험군 환자를 따로 분류하고 치료 기준을 세분화하여 치료가 필요한 환자에서 투약이 지연되지 않는 것을 목표로 하였다. 그러나 국내에 적합한 스타틴의 용량 및 LDL 콜레스테롤 농도의 목표, 일차 예방의 기준이 되는 위험인자 및 고중성지방혈증의 조절 목표에 관해서는 국내 인구 집단을 대상으로 한 추가적인 연구가 필요할 것으로 생각되며 이를 통해 향후 국내에 적합한 치료지침을 정할 수 있을 것으로 생각된다.
텍스트 추가

대표사진 삭제
사진 설명을 입력하세요.
텍스트 추가
과거 국내 치료지침에서는 투약 전 지질 검사를 시행하고 투약 6주 이후나 용량 조절 시 다시 지질 검사를 할 것을 권고하고 있었다. 2013 ACC/AHA1 치료지침에서는 스타틴 투약에 대한 무작위 배정 연구 결과들을 고려하여 투약하기 전 지질 검사(총콜레스테롤, 중성지방, HDL 콜레스테롤, LDL 콜레스테롤 등을 포함)를 시행하고 투약시작 1–3개월 후에 다시 지질 검사를 시행해서 호전 여부를 평가할 것을 추천하고 있다. 또한 그 이후에는 지질 검사 결과가 목표에 도달했는지 여부에 따라 3–12개월 간격으로 추적 관찰할 것을 권고하고 있다. 2011 ESC/EAS5 치료지침에서는 투약 시작 6–8주에 지질 검사를 하고 잘 조절되는 경우에 6–12개월 추적 검사를 시행할 것을 권장하고 있다. 이번 개정된 지침에서도 기존의 국내 지침 및 국외의 지침들을 고려하여 투약 전 지질 검사를 시행하고 투약시작 –12주 후에 다시 지질 검사를 시행해서 투약에 대한 반응 및 순응도를 평가하는 것을 추천하며 이후에는 환자의 심혈관계 위험도 및 투약 후 지질 강하 정도에 따라 3–12개월 간격으로 지질 검사를 시행하는 것을 권고한다(I, A).
스타틴 투약 후 간기능 검사에 대한 기존의 추적관찰 기준을 살펴보면 이전 국내 지침에서는 투약 전 간기능 검사를 하고, 투약 후 6주와 12주에 다시 검사를 시행하며 이상이 없을 시에는 이후부터 6개월마다 반복해서 시행할 것을 권고했으며, 간효소 수치가 3배 이상 증가되는 것이 확인되면 투약을 중단하는 것을 추천했었다. 2011 ESC/EAS 치료지침 및 이전 JUPITER6, CARDS7와 같은 무작위 배정 연구들에서도 스타틴을 투약하기 전 간효소 수치를 측정하고, 투약을 시작했거나 증량한 경우 2달 뒤에 다시 측정할 것을 권고했으며 간효소 수치가 2번 연속 검사에서 정상의 3배 이상 상승되었을 때 투약 중단을 권고하였던 점을 고려하면 기존의 국내 지침과 현재 국외의 지침들에 큰 차이가 없는 것으로 생각된다. 개정된 지침은 지질 검사와 동시에 시행하는 것을 권고한다(I, B).
또한 기존 국내 치료지침에서는 스타틴 투약 후 근육통, 근무력감 등을 호소하면서 creatinine kinase (CK) 수치가 정상치의 10배 이상 증가하는 경우 근육병증으로 진단하며 투약을 중단할 것을 권고했는데 2013 ACC/AHA1 및 이전의 무작위 배정 연구들에서도 국내 지침과 유사하게 스타틴을 투약하기 전 CK 농도를 측정하고 투약 후 CK 농도가 정상상한치의 10배 이상 상승되며 증상이 동반되는 경우 투약을 중단할 것을 권고하였다. 따라서 개정된 지침에서도 이전 지침을 유지하여 근육병증의 증세가 동반되는 경우 CK 수치를 확인하여 10배 이상 증가하는 경우 투약을 중단하는 것을 권고한다(II, A). 또한 환자의 안전을 위해 증상이 없더라도 의사의 판단에 의해 추적검사를 할 수 있다(IIb, E).
이전 국내 치료지침에서는 fibrate 및 nicotinic acid를 투약한 후 추적관찰에 대해서는 언급이 되어있지 않았으며 아직 확실하게 국내 및 국외의 기준이 정해지지는 않은 상태이다. 이전 FIELD 연구에서는 fenofibrate 투약군의 평균 혈중 크레아티닌 수치는 1.03 mg/dL, 위약군은 0.90 mg/dL로 투약군에서 더 높은 수치가 확인되었으며, ACCORD 연구에서도 fenofibrate를 statin에 추가 투약한 군에서 혈중 크레아티닌 수치가 0.93 mg/dL에서 1.10 mg/dL로 상승했으나 statin 단독 투약군에서는 0.93 mg/dL에서 1.04 mg/dL로 확인되어 동시 투약군에서 혈중 크레아티닌 수치가 경도의 상승을 보인 바 있었다. 위의 두 연구에서 fibrate 투약군에서 알부민뇨의 진행은 감소하는 소견을 보였다. 2013 ACC/AHA 치료지침에서는 이전 연구 결과들을 고려해서 투약 전 혈중 크레아티닌 수치 및 사구체 여과율(eGFR)을 통해 신장기능을 평가하고 투약 시작 후 3개월 및 이후 6개월마다 신장기능을 재평가할 것을 권고하였다.1 이후 지속적으로 사구체 여과율이 30 mL/min/1.73 m2 미만으로 확인될 경우 투약 중단을 권고하며, 30에서 59 mL/min/1.73 m2 사이일 때는 투약용량이 54 mg/day가 넘지 않게 조절하는 것을 추천한 바 있었다. 이와 같은 지침 및 이전의 연구 결과들을 고려할 때 국내에서도 fibrate 투약 전 및 투약 3개월 후에는 혈중 크레아티닌 수치를 확인하는 것을 권고하며 이후에 이상이 없다면 6개월마다 추적관찰하는 것이 적합할 것으로 생각된다(II, B).
'내분비내과 > 이상지질혈증' 카테고리의 다른 글
| Evolocumab 주사제(품명: 레파타주 프리필드펜), 요양급여 기준과 적응증, 기전프로파일 (0) | 2019.11.11 |
|---|---|
| 이상지질혈증에서 혈액검사 모니터링 (0) | 2019.10.13 |
| 제1장 한국인 이상지질혈증의 역할 [2018 이상지질혈증 치료지침 제4판] (0) | 2019.09.29 |
| Clinical risk factors for stroke, TIA, and systemic embolism in the CHA2DS2-VASc score (0) | 2019.08.25 |
| Characteristic findings of different genetic causes of hypercholesterolemia (0) | 2019.08.24 |



